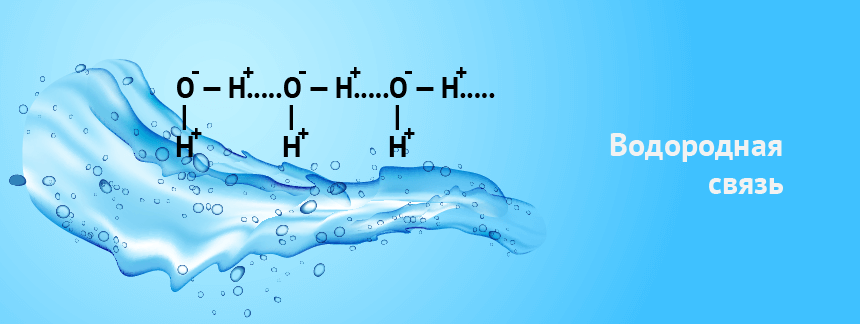
Как известно, атомы, имеющие большую электроотрицательность, имеют тенденцию притягивать к себе электроны менее электроотрицательного партнера, давая ему низкий положительный заряд (σ+). В случае с водородом этот заряд позволяет ему взаимодействовать с другим атомом. У второго атома должны присутствовать неподеленные электронные пары, которые позволят ему взаимодействовать с водородом. Механизм образования связи схож с ковалентной и может быть рассмотрен в качестве ее варианта.
Это связь, образующаяся между атомом водорода, который уже связан с атомом, имеющим высокую электроотрицательность, и другим электроотрицательным атомом.
Можно представить структуру обсуждаемого явления так: сравнительно большие электроотрицательные атомы — это двое взрослых, которые держат за руки малыша-водорода. Наиболее распространенные кандидаты на роль «родителей» — это фтор, кислород и азот.
Свойства и типы водородных связей
Ковалентная и водородная связь сильно различаются по силе. Водородная значительно слабее, однако ее энергия и стабильность выше, чем у слабых межмолекулярных взаимодействий, таких как силы Ван-дер-Ваальса. Образование и разрушение водородной связи не требуют значительных затрат энергии, и она является достаточно стабильной при нормальных условиях. Подобная гибкость, обуславливает ее широкое распространение в молекулах, используемых живыми организмами, – «сборка» и «разборка» таких молекул легко осуществляется силами естественных энзимов. Можно выделить два подтипа обсуждаемой связи:
- внутримолекулярная – образуется между атомами одной молекулы;
- межмолекулярная – между атомами двух молекул.
Чтобы лучше понять, что к чему, давайте рассмотрим каждую из них.
Водородная связь: примеры
Две цепи ДНК, соединенные между собой при помощи большого количества водородных связей, — один из самых очевидных примеров внутримолекулярной водородной связи в биомолекулах. В процессе копирования, записи и восстановления генетической информации связи между цепями разрываются и соединяются множество раз на ограниченном участке молекулы.
Примерами веществ, между которыми образуются водородные связи могут служить спирты. Водородные связи, образующиеся между отдельными молекулами спиртов, обеспечивают им высокие точки кипения и плавления. Молекулы спиртов «держатся» друг за друга при помощи водородных связей, образуя более устойчивую структуру. Больше водородных связей – больше энергии необходимо для доведения вещества до кипения.
Обсуждаемые связи могут образовываться и между неорганическими молекулами, например, между молекулами воды. Рассмотрим этот случай подробнее.
Водородные связи в воде
Для начала давайте вспомним, как выглядит молекула воды. Она представляет собой атом кислорода, связанный с двумя атомами водорода и имеющий две неподеленные электронные пары – H2O. Каждый из атомов водорода может образовать связь с еще одной молекулой, из-за чего вода приобретает некоторые интересные свойства.
В числе прочего такая организация, позволяет воде иметь более высокую температуру кипения. Механизм достижения подобной стабильности по сути такой же, как и в спиртах. При температурах, превышающих ноль по шкале Цельсия, но ниже температуры кипения, молекулы воды образуют структуры, подобные изображенной на рисунке выше, но они представляют собой отдельные конгломерации, а не целостную структуру. При низкой температуре вода образует лед, в котором водородные связи присутствуют в полном объеме, образуя решетку. Ячейки решетки крупнее, чем молекула воды, что обеспечивает еще одно интересное свойство – более низкую плотность в твердом агрегатном состоянии.
Вода является отличным растворителем.
Полярные молекулы воды легко реорганизуются вокруг положительно или отрицательно заряженных ионов, поворачиваясь к ним соответствующей стороной. Особенно хорошо в воде растворяются другие водородосодержащие соединения, способные к образованию водородных связей с молекулами воды и самими собой. Поэтому спирты, а также аммиак и некоторые другие соединения способны растворяться в воде в колоссальных объемах.
Вам нужно срочно заказать статью по химии для публикации? Обратитесь за помощью к нашим экспертам!



Комментарии 1
Cырой и неупорядоченный текст на уровне ученика 9 класса. Например, автор пишет о внутримолекулярной связи, а в качестве примера рассматривает образование водородной связи между двумя цепями ДНК. И, самое главное, нет доходчивого объяснения образования водородной связи. Пример неудачного текста: "Полярные молекулы воды легко реорганизуются вокруг положительно или отрицательно заряженных ионов, поворачиваясь к ним соответствующей стороной".