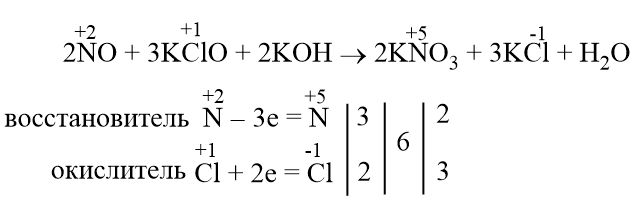Материалы по запросу: расставьте коэффициенты методом электронного баланса
146. Расставьте коэффициенты в окислительно-восстановительных реакциях, в первой методом электронного баланса, во второй — электронно-ионного баланса: F₂ + H₂O ⟶ HF + O₂; PH₃ + KMnO₄ + H₂SO₄ ⟶ H₃PO₄ + MnSO₄ + K₂SO₄ + H₂O.
146. Расставьте коэффициенты в окислительно-восстановительных реакциях, в первой методом электронного баланса, во второй — электронно-ионного баланса: F₂ + H₂O ⟶ HF + O₂; PH₃ + KMnO₄ + H₂SO₄ ⟶ H₃PO₄ +
Пользуясь методом электронного баланса, расставьте коэффициенты в уравнениях окислительно-восстановительных реакций
Пользуясь методом электронного баланса, расставьте коэффициенты в уравнениях окислительно-восстановительных реакций
ТГАСУ. Химия. ч. 2. Химические свойства металлов
уравнение реакции алюминия с соляной кислотой. Используя метод электронного баланса, расставьте коэффициенты в реакции. Какая сумма коэффициентов получилась? В каком соотношении по массе следует взять две
Расставить коэффициенты методом электронного баланса : FeO+HNO3=>Fe(NO3)3+NO+H2O Расставить коэффициенты…
Расставить коэффициенты методом электронного баланса : FeO+HNO3=>Fe(NO3)3+NO+H2O Расставить коэффициенты методом электронного баланса : FeO+HNO3=>Fe(NO3)3+NO+H2O
Ответ на вопрос
Сначала запишем несбалансированное уравнение:FeO + HNO3 => Fe(NO3)3 + NO + H2OТеперь составим уравнение с учетом изменения степеней окисления:FeO + 8HNO3 => Fe(NO3)3 + NO + 4H2OСбалансируем уравнение, начав с атомов кислорода:FeO + 8HNO3 => Fe(NO3)3 + NO + 4H2OТеперь балансируем атомы азота:FeO + 8HNO3 => Fe(NO3)3 + NO + 4H2OИ, наконец, балансируем атомы железа, чтобы уравнение было полностью сбалансировано:FeO + 8HNO3 => Fe(NO3)3 + NO + 4H2OТаким образом, коэффициенты равны:
FeO + 8HNO3 => Fe(NO3)3 + NO + 4H2O.
Еще
102
1
[ОТВЕТЫ] Синергия Регулирование финансово-кредитной деятельности.фэ_БАК🟢 Итоговый тест Экзамен
· 5 электронное сообщение на интернет-сайт Президента РФ Для снижения размера возможных потерь система лимитов относится к … · методам выявления риска · методам оценки
Регулирование финансово-кредитной деятельности.фэ_БАК (новый) тест с ответами Синергия/МОИ/ МТИ /МОСАП
денежных средств и их использовании; E.Отчёт о финансовых результатах (ОКУД 0409807) F.Бухгалтерский баланс (ОКУД 0409806) G.Сведения об обязательных нормативах, нормативе финансового ры-чага и нормативе краткосрочной
💯 Регулирование финансово-кредитной деятельности.фэ_БАК [Занятие] (ответы на тест Синергия / МОИ / МТИ / МосАП, март 2024)
краткосрочной ликвидности (ОКУД 0409813) F. Отчёт о финансовых результатах (ОКУД 0409807) G. Бухгалтерский баланс (ОКУД 0409806) H. Отчёт о движении денежных средств (ОКУД 0409814) В Российской Федерации в 2024
Расставьте коэффициенты методом электронного баланса K2MnO4+Na2SO3+H2O=MnO2+Na2SO4+KOH
Расставьте коэффициенты методом электронного баланса K2MnO4+Na2SO3+H2O=MnO2+Na2SO4+KOH
183
1
Расставить коэффициенты методом электронного баланса, указать окислители и восстановители: Расставить…
Расставить коэффициенты методом электронного баланса, указать окислители и восстановители: Расставить коэффициенты методом электронного баланса, указать окислители и восстановители: KCrO2 + H2O2 + KOH
Ответ на вопрос
1) KCrO2 + 4H2O2 + 2KOH = 2K2CrO4 + 3H2O (окислитель - KCrO2, восстановитель - H2O2)
2) 2SO2 + 2HNO3 = 2NO2 + 2H2SO4 (окислитель - HNO3, восстановитель - SO2)
Еще
71
1
Расставить коэффициенты методом электронного баланса Li2s + H2SO4 = LiHSO4 + SO2 + S + H2O…
Расставить коэффициенты методом электронного баланса Li2s + H2SO4 = LiHSO4 + SO2 + S + H2O
Ответ на вопрос
Сначала записываем неизвестные коэффициенты в уравнение:a Li2S + b H2SO4 = c LiHSO4 + d SO2 + e S + f H2OТеперь начнем балансировку уравнения:Балансируем атомы серы: на правой стороне у нас есть только один атом серы в LiHSO4, следовательно, e = 1.
Теперь у нас уравнение выглядит так:
a Li2S + b H2SO4 = c LiHSO4 + d SO2 + S + f H2OБалансируем атомы лития: на левой стороне у нас два атома лития, значит, a = 2.
Теперь у нас уравнение выглядит так:
2 Li2S + b H2SO4 = c LiHSO4 + d SO2 + S + f H2OБалансируем атомы кислорода: на левой стороне у нас 4 кислорода в H2SO4 и 2 кислорода в Li2S, так что всего у нас 6 кислородов. На правой стороне у нас 4 кислорода в H2O и 4 кислорода в LiHSO4, т.е. всего 8 кислородов. Значит, на левой стороне нам нужно добавить еще 2 кислорода. Добавляем одну молекулу O2 и получаем:
2 Li2S + b H2SO4 = c LiHSO4 + d SO2 + S + 2 H2OТеперь балансируем атомы водорода: на левой стороне у нас 4 водорода в H2SO4 и 4 водорода в H2O, а значит, b = 2 и f = 2.
Итак, окончательное сбалансированное уравнение выглядит следующим образом:2 Li2S + 2 H2SO4 = c LiHSO4 + d SO2 + S + 2 H2OОтвет: 2 Li2S + 2 H2SO4 = 2 LiHSO4 + SO2 + S + 2 H2O
Еще
82
1
Естествознание СОО (ДО, СпДО, ПНК, КП, ПДО, ДОУА)
Для расстановки коэффициентов в ОВР используют метод электронного баланса, суть которого заключается в том, что количество электронов, отданных восстановителями равно количеству электронов, принятых окислителями
Расставить коэффициенты методом электронного баланса. Определить окислитель и восстановитель. 1)Ag + O2…
Расставить коэффициенты методом электронного баланса. Определить окислитель и восстановитель. 1)Ag + O2 = Ag2O 2) Li + HCl = LiCl + H2
Ответ на вопрос
1) Ag + 1/2 O2 = Ag2OAg: 0, Ag2O: 1, O2: -1/2Окислитель: O2
Восстановитель: Ag2) 2 Li + 2 HCl = 2 LiCl + H2Li: 0, HCl: 0, LiCl: 0, H2: 0Окислитель: HCl
Восстановитель: Li
Еще
106
1
ОЦЕНОЧНАЯ ДЕЯТЕЛЬНОСТЬ//СИНЕРГИЯ/МТИ//МОИ//ОТВЕТЫ ВЫДЕЛЫ ЖЕЛТЫМ
уникальных, специализированных объектов машин и оборудования предпочтительным является использование методов … подхода доходного сравнительного затратного 7. Оценочная методология, соответствующая цели оценки
. Расставить коэффициенты методом электронного баланса, указать окислитель и восстановитель: . Расставить…
. Расставить коэффициенты методом электронного баланса, указать окислитель и восстановитель: . Расставить коэффициенты методом электронного баланса, указать окислитель и восстановитель:
Ответ на вопрос
Сначала выписываем уравнение реакции:
Fe2O3 + 3CO → 2Fe + 3CO2Теперь определяем окислитель и восстановитель:
Окислителем является CO, поскольку он передает кислород Fe2O3 для образования CO2, тем самым сам восстанавливаясь до CO2. Восстановителем же является Fe2O3, так как он принимает кислород от CO, восстанавливаясь до Fe.Теперь расставляем коэффициенты методом электронного баланса:
Fe2O3 + 3CO → 2Fe + 3CO2Таким образом, окислитель - CO, восстановитель - Fe2O3.
Еще
32
1
Расставить коэффициенты методом электронного баланса Mn+H2SO4— MnSO4+S+H2O
Расставить коэффициенты методом электронного баланса Mn+H2SO4— MnSO4+S+H2O
Ответ на вопрос
Для расстановки коэффициентов методом электронного баланса в реакции Mn + H2SO4 → MnSO4 + S + H2O, сначала определим окислительно-восстановительные номера для каждого элемента:Mn: x
H: +1
S: +6Теперь составим уравнения полуреакций для окисления и восстановления:Окисление:
Mn → Mn2+ + 2e- (окислительное число Mn уменьшается с x до +2)Восстановление:
S6+ + 6e- → S (окислительное число S уменьшается с +6 до 0)Теперь сбалансируем количество передаваемых электронов в двух полуреакциях:Для ионов Mn2+ и S: 2е- - 6е- = 12e-Следовательно, для сбалансированной реакции необходимо умножить каждую полуреакцию на 6:6Mn + 6H2SO4 → 6MnSO4 + 3S + 6H2OТаким образом, коэффициенты для данной реакции, рассчитанные методом электронного баланса, равны: 6Mn, 6H2SO4, 6MnSO4, 3S, 6H2O.
Еще
119
1
Электронный баланс (жесткое окисление) Расставить коэффициенты методом электронного баланса CH2=CH-CH=CH2+KMnO4+H2SO4…
Электронный баланс (жесткое окисление) Расставить коэффициенты методом электронного баланса CH2=CH-CH=CH2+KMnO4+H2SO4
Ответ на вопрос
Начнем с нахождения окислителя и восстановителя.
CH2=CH-CH=CH2 - вещество, которое будет окисляться (вещество, потребляющее электроны).
KMnO4 - окислитель (вещество, отдавающее электроны).Составим уравнение реакции и определим количество электронов, участвующих в процессе окисления и восстановления:
CH2=CH-CH=CH2 + KMnO4 + H2SO4 -> ??? + ??? + ???Метод электронного баланса:
CH2=CH-CH=CH2 -> 4 электрона (2 для каждого двойного связывания)
KMnO4 -> 5 электронов (согласно структурной формуле)
Сумма: 4 + 5 = 9 электроновПодберем коэффициенты перед веществами так, чтобы суммарное количество электронов совпало:
CH2=CH-CH=CH2 + 9/4 KMnO4 + ??? -> ??? + 9/4 Mn^2+ + ??? + ???.Итак, получаем уравнение реакции:
CH2=CH-CH=CH2 + 9/4 KMnO4 + H2SO4 -> 4CO2 + 6H2O + 9/4 Mn^2+ + K2SO4. Таким образом, уравнение реакции после балансировки с учетом электронного баланса будет:
C4H8 + 9/4 KMnO4 + H2SO4 -> 4CO2 + 6H2O + 9/4 Mn^2+ + K2SO4.
Еще
182
1
[на 25 баллов из 25] Практическое занятие 3 по естествознанию (НСПК)
Для расстановки коэффициентов в ОВР используют метод электронного баланса, суть которого заключается в том, что количество электронов, отданных восстановителями равно количеству электронов, принятых окислителями
Химия окислительный процесс пж Расставьте коэффициенты методом электронного баланса в уравнении реакции…
Химия окислительный процесс пж Расставьте коэффициенты методом электронного баланса в уравнении реакции взаимодействия натрия и фосфора
26
1
[Росдистант] Экономика организации 2 (промежуточные и итоговый тесты, вопросы, ответы)
или несколько ответов: Технологией и техническими средствами планирования Совокупностью приемов и методов планирования Перспективными и текущими планами Оперативными планами Образование резервного фонда
Расставьте коэффициенты методом электронного баланса. Определитель окислитель, восстановитель. NO+KCLO+KOH->KNO3+KCL+H2O…
Расставьте коэффициенты методом электронного баланса. Определитель окислитель, восстановитель. NO+KCLO+KOH->KNO3+KCL+H2O
299
1
Что часто ищут
Поможем написать учебную работу